date:2026-03-23 11:45:11
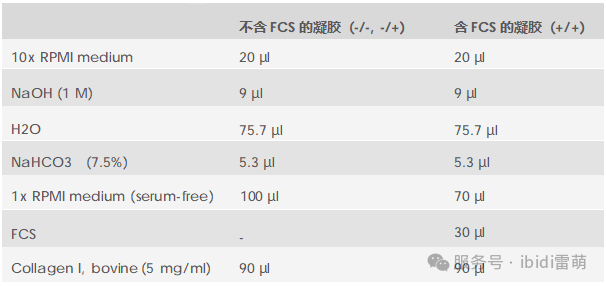
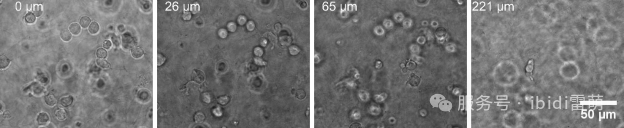
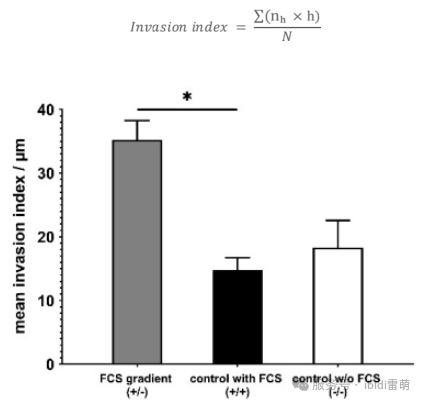
理解細胞侵襲對于揭示腫瘤進展和免疫細胞遷移的機制至關重要,這兩者都是疾病發展和治療反應的核心。本方案描述了一種趨化性驅動的侵襲實驗,使用3D自插式微孔插件 (micro-Inserts 3D for self-insertion),插件內并填充I型膠原蛋白(collagen I)基質,用于評估Jurkat T細胞的遷移行為。 代表快速遷移淋巴細胞的Jurkat細胞被接種在膠原凝膠的頂部,并通過相鄰儲液池中不同濃度的胎牛血清(FCS)產生的血清梯度進行刺激。24小時后,通過成像和深度量化評估細胞向膠原基質內的侵襲情況。與化學均質環境中的細胞相比,暴露于FCS梯度的細胞顯示出顯著更深的侵襲,這與血清的絕對存在與否無關。 該設置模擬了3D環境中的趨化性侵襲,突顯了方向性信號在促進細胞通過細胞外基質組分進行主動遷移中的作用。該方案提供了一個強大且可重復的平臺,用于在生理相關條件下研究免疫細胞遷移和腫瘤微環境相互作用。 1.1 試劑和緩沖液 3D自插式微孔插件micro-Inserts 3D for self-insertion (80499, ibidi GmbH) μ-Plate 24 Well, ibiTreat (82426, ibidi GmbH) Collagen Type I, Bovine (I型膠原,牛源) (50303, ibidi GmbH) Jurkat細胞(ACC 282, DSMZ GmbH) RPMI 1640培養基(21875034, Gibco, Thermo Fisher Scientific) 胎牛血清(FCS, 10270106, Gibco, Thermo Fisher Scientific) 10× RPMI 1640培養基 (R1145, Sigma) 超純水配制的NaOH (1 M) NaHCO?7.5% (S8761, Sigma) 無菌超純水 1.2 設備 細胞培養箱(加濕,37°C,5% CO?) 標準細胞培養設備(無菌操作臺,細胞消化試劑盒,培養瓶,帶合適吸頭的移液器等) 冷卻的鋁珠或冰塊 每個實驗需制備三種不同的樣本,每種樣本均設置三個重復: 1.梯度樣品 (-/+):僅在micro-Insert 3D的外側孔中添加趨化因子(本例中為10% FCS)。 2.均一分布樣品 (+/+):整個樣品(即外側孔、內側孔和凝膠基質中)均含有10% FCS。 3.無趨化因子樣品 (-/-):培養基和凝膠中均不添加FCS。 圖1:三種實驗條件的示意圖(上:-/+,中:+/+,下:-/-):細胞被接種在3D微孔插件內的3D膠原基質上。上(-/+):在微孔插體的外側孔中加入趨化因子溶液,并讓細胞侵入基質1-3天(具體時間取決于細胞類型)。中(+/+):在微孔插體的內側和外側孔中均加入趨化因子溶液(形成均一濃度環境)。下(-/-):未加入任何趨化因子。 2.1 樣本制備 將九個micro-Inserts 3D分別放入µ-Plate 24 well 24孔培養板的孔中。輕輕按壓每個插件以去除截留的氣泡,并確保其與表面牢固接觸。 向培養板的空余孔中填充無菌水或PBS,以減少孵育期間的蒸發。 2.2 膠原凝膠制備 在開始制備凝膠前,請閱讀I型膠原蛋白(Collagen Type I)說明書。 本實驗需要制備兩種膠原凝膠混合物: 不含血清(用于-/+和-/-樣品) 含10%胎牛血清(FCS)(用于+/+樣品) 重要提示:膠原凝膠的移液操作 進行膠原凝膠移液時,請務必使用預冷的移液器吸頭(4°C)。 對于I型膠原凝膠的制備,由于凝膠粘度高,建議所有步驟均采用反向移液法。將移液器按壓至第二壓力點,使整個吸頭充滿凝膠。排液時僅需按壓至第一壓力點,雖然此時槍頭內會殘留少量膠原液(需棄去),但這種方法能確保排出的膠原體積更加精確。我們推薦使用Eppendorf Visco Tips或Gilson Microman E等產品。 請注意,即使在4°C下,凝膠混合物也最多只能在5分鐘內使用,之后便會開始部分凝膠。 1.按照表1的配比,制備膠原混合液(1.5 mg/ml牛源膠原,含或不含10%血清)。請按表1所列順序添加各組分,并用移液器充分混勻,操作時置于冰上以延緩凝膠化。 2.向每個micro-Insert 3D的內側孔中加入20 μl混合液。為確保形成平整的膠原層,將移液器垂直對準孔中央進行加樣。 3.蓋上培養板蓋子,將培養板放入培養箱中聚合約30分鐘。 注意:如需便捷地計算不同膠原濃度,可直接使用ibidi官網提供的ibidi膠原濃度計算器(ibidi Collagen Calculator)。 表1:配制300 μl含或不含FCS的1.5 mg/ml I型膠原基質的移液方案 2.3 細胞接種 1.在凝膠聚合期間,按常規方法收集細胞。 2.制備兩份細胞懸液,濃度為3 × 10?細胞/ml: 細胞懸液1:使用無血清培養基(用于 -/- 和 -/+ 樣品) 細胞懸液2:使用含10% FCS的培養基(用于 +/+ 樣品) 3.從培養箱中取出培養板,在顯微鏡下確認凝膠聚合情況。如果基質未完全聚合,可再孵育10-15分鐘。 4.按以下方式向每個micro-Insert 3D的外側孔中填充250 μl培養基: 對于 -/- 樣品:使用無血清培養基 對于 -/+ 和 +/+ 樣品:使用含10% FCS的培養基 5.向每個孔的凝膠基質上方加入25 μl相應的細胞懸液。注意避免移液器吸頭觸碰凝膠基質。 6.蓋上培養板蓋子,將培養板放回培養箱。讓細胞侵入凝膠24小時。 3. 成像 1.24小時后,使用相差顯微鏡記錄細胞在凝膠基質中的侵襲情況。 2.對于每個micro-Insert 3D插件中部選擇三個隨機的XY位置(膠原層平整處)。在每個位置采集一個z-stack,從凝膠頂部(細胞聚焦處)開始,一直掃描到孔的底部,Z軸步長為13 µm。 注意: 相鄰圖像之間的z間隔應大致等于單個細胞的直徑(約8–15 µm),以確保最終圖像堆棧中能捕獲所有細胞。 圖 2:在FCS梯度(-/+)條件下,Jurkat細胞浸潤進入凝膠基質24小時的Z軸堆疊掃描(z-stack)代表性圖像。在micro-Insert 3D內的同一位置,于不同Z平面上采集的相差顯微鏡圖像。第一張圖像(0 µm)顯示細胞位于凝膠基質頂部。在隨后的圖像中,只有浸潤到指定深度的細胞處于聚焦狀態。圖像使用Zeiss Axio Observer Z1顯微鏡配備40× LD Plan-Neofluar物鏡拍攝。 為評估細胞對趨化因子FCS的侵襲響應,需為每個孔計算一個深度分數,該分數基于各z平面圖像中處于焦平面的細胞數量,反映細胞向基質內的侵襲深度。 侵襲指數的計算方法為:將每個深度h處(nh)的(處于焦平面的)細胞總數乘以對應的深度h(單位為µm),并除以所有深度內細胞的總數(N): 圖3:Jurkat細胞在FCS梯度下的趨化驅動侵襲。柱狀圖顯示平均侵襲指數。數據表示24小時后的平均值+SEM(標準誤)(n = 2個獨立實驗,每個實驗重復三次)。結果顯示,與處于FCS濃度均一環境下的樣本相比,暴露于FCS梯度的細胞向膠原基質內的侵襲深度顯著更深。注:在本示例中,對于橫跨多個層面(slices)的細胞,僅在細胞中心平面聚焦的層面進行一次計數。 5. 總結 這種使用micro-Insert 3D進行的趨化性驅動侵襲實驗,為定量分析3D膠原基質中的免疫細胞遷移提供了一種可靠且具有生理相關性的方法。在不同血清條件下觀察到的浸潤深度差異,突顯了方向性信號(directional cues)在細胞運動中的重要性。該方案非常適用于趨化行為的對比研究,并可針對其他細胞類型或趨化因子進行調整,從而探索細胞侵襲及微環境相互作用的多個維度。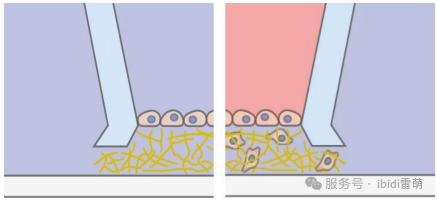


ICP備案號:
滬ICP備15057650號-1
 滬公網安備31011202005471
滬公網安備31011202005471
雷萌生物科技(上海)有限公司 保留所有版權.